Unterrichtsmaterialien Chemie: Reaktions- und Bildungsenthalpie
15 MaterialienIn über 15 Dokumenten und Arbeitsblättern für das Fach Chemie: Reaktions- und Bildungsenthalpie findest du schnell die passenden Inhalte für deine nächste Stunde. Jetzt kostenlos testen und mehr Materialien nach der Anmeldung entdecken!
Auswählen
Auswählen
Auswählen
Auswählen
15 Materialien
Einheit
Welche Inhalte sollen bearbeitet werden?Fachkompetenz Chemie – Leitlinien – Basiskonzepte (PP); Basiskonzept Stoff-Teilchen (PP); Basiskonzept Struktur-Eigenschaft (PP); Leitlinie Stoff-Struktur-Eigenschaften (PP); Basiskonzept Chemische Reaktion (PP); Beispiele für dasDonator-Akzeptor-Konzept(PP); Basiskonzepte Energie bzw. ChemischesGleichgewicht(PP); Leitlinie Chemische Reaktion (PP); Erkenntnisse gewinnen (KS); Weg der Erkenntnisgewinnung (KS); LeitlinieDenk- und Arbeitsweisen der Chemie (KS); Didaktische Reduktion (BR, PP); Maßnahmen zur Didaktischen Reduktion (BR, PP); Leitlinie Historische Betrachtungsweise (PP); Didaktische Prinzipien der Stoffauswahl und -anordnung (AK); Didaktisches Prinzip der Lernzielorientierung (AK); Didaktisches Prinzip der Schülerangemessenheit (AK); Didaktisches Prinzip des Exemplarischen Lehrens und Lernens (AK); Leitlinie „Bezug zur Lebenswelt“ (PP, KS)
Testen kostet nichts
Probiere meinUnterricht 14 Tage lang aus. Kündigst du während deiner Probezeit, entstehen für dich keine Kosten. 🚀
Einheit
Reaktionen von Gasen genauer untersuchen - Qualitative und quantitative Versuche mit der SpritztechnikDer Einsatz von Spritzen ist besonders gewinnbringend, wenn dabei das Verschwinden von Gasen, wie z. B. bei der Reaktion von Metallen mit Sauerstoff, sichtbar werden soll oder die Bildung gasförmiger Reaktionsprodukte, wie z. B. von Wasserstoff, für weitere Erkenntnisse bezüglich der ablaufenden Reaktion dienen kann. Dies möchten wir an drei Beispielen exemplarisch genauer aufzeigen.
Einheit
Aluminothermische Bronze - Mit brisanter Gitterenergie zum alchimistischen GoldAluminothermische Bronze - Mit brisanter Gitterenergie zum alchimistischen Gold
Einheit
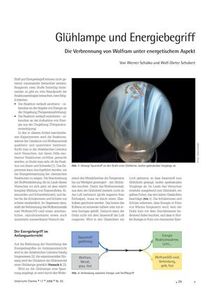
Glühlampe und Energiebegriff - Die Verbrennung von Wolfram unter energetischem AspektIn den in diesem Artikel beschriebenen Experimenten wird die Reaktionswärme der Oxidation von Wolframmetall qualitativ und quantitativ bestimmt. Sucht man in der didaktischen Literatur nach Versuchen, mit deren Hilfe exotherme Reaktionen sichtbar gemacht werden, so findet man sehr oft die Reaktion von Eisen und Schwefel. Das Experiment kann durchgeführt werden,um die Energiefreisetzung bei chemischen Reaktionen zu zeigen. Die Beschreibung der Stoffveränderung, die im Laufe dieses Versuches vor sich geht, ist aber relativ komplex (Bildung von Eisensulfiden, Eisenoxiden und Schwefeldioxid), und daher für die Schülerinnen und Schüler nur schwer verständlich. Im Gegensatz dazu, stellt die Verbrennung des Wolframmetalls zum Wolfram(VI)-oxid einen anschaulichen, reproduzierbaren sowie auch quantitativ auswertbaren Versuch dar.
Verwandte Themen
Einheit
Kupfer entstehen lassen - Von Kupfer über Zwischenverbindungen wieder zum KupferIn diesem Artikel werden Reaktionen vorgestellt, die das elementare Kupfer in verschiedene chemische Verbindungen überführen und in einer oder in mehreren Zwischenstufen zum Kupfer zurückführen. Diese Vorgänge beinhalten nicht nur die Gewinnung des Kupfers aus dem Kupfererz und das Recycling von Kupfer, sondern es wird auch das „Wesen“ chemischer Vorgänge angesprochen. Schließlich verschwindet das Metall Kupfer scheinbar in einer Verbindung und obwohl es nicht mehr sichtbar ist, so steckt es doch in einer anderen Form (Ionen) darin und kann wieder als Metall „herausgeholt“ werden. Besonders dem Chemieanfänger erscheint es sonderbar, dass in einer grünen, wässrigen Lösung von Kupferchlorid noch Kupfer in irgendeiner Form enthalten sein soll. Die Umwandlung einer chemischen Kupferverbindung in eine andere Kupferverbindung kann also ohne Zweifel spannend sein.
Einheit
Reaktionsenergie sichtbar gemacht - Energetische Betrachtungen bei der Bildung von EisensulfidReaktionsenergie sichtbar gemacht - Energetische Betrachtungen bei der Bildung von Eisensulfid
Einheit
Chemische Reaktionen – Bildung neuer Stoffe - Teil 1Sicherheitshinweise; Fachliche Hinweise; Didaktische Hinweise; Tabellarischer Ablauf; Protokoll: Kennzeichen einer chemischen Reaktion; Lerntheke 1: Auswertung der Versuche; Lerntheke 2: Wir forschen weiter; Lerntheke 3: Recherche
Testen kostet nichts
Probiere meinUnterricht 14 Tage lang aus. Kündigst du während deiner
Probezeit, entstehen für dich keine Kosten. 🚀
Probezeit, entstehen für dich keine Kosten. 🚀